

1 способ. Пассивная защита от коррозии – изолирование поверхность металла с помощью диэлектрического покрытия. В этом случае выход электронов в раствор исключен.
Именно этот способ применяют, нанося защитные полимерные покрытия на трубопроводы, используемые для укладки в грунте.
2 способ. Активная защита от коррозии – для защиты металла трубы на дефектных участках изоляции применяется второй способ – так называемая катодная защита от коррозии.
При электрохимической коррозии разрушение металла происходит за счет выхода ионов металла в раствор. Затормозить этот процесс можно за счет «насыщения» металла электронами, которые в паре с катионами раствора создадут барьер, препятствующий выходу ионов.
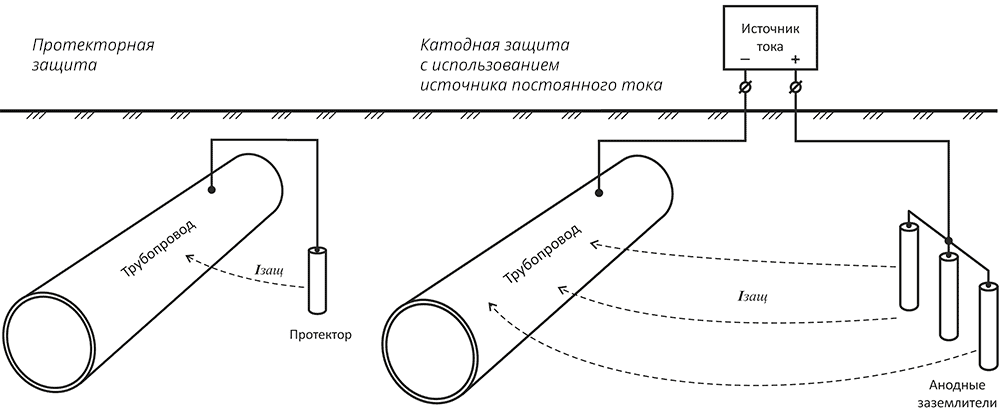
Виды активной (катодной) защиты от электрохимической коррозии
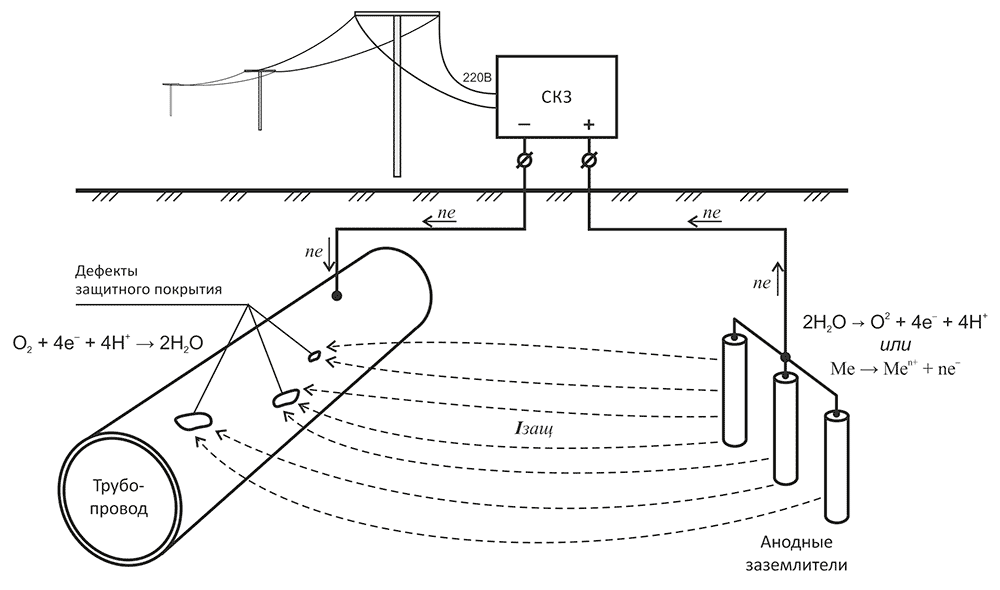
Схема катодной защиты
При катодной защите в результате прохождения постоянного тока через грунт, происходит электролиз грунтового электролита. Положительно заряженные ионы (катионы) перемещаются к катоду (трубопроводу), а отрицательно заряженные ионы (анионы) движутся в направлении от катода к аноду (анодному заземлителю).
Преобразование тока осуществляется за счет следующих электрохимических реакций.
На металле трубопровода в местах нарушения защитного покрытия протекает реакция восстановления растворенного в воде кислорода:
О2 + 4е- + 4Н+ → 2Н2О (К)
На анодном заземлении возможно протекание следующих реакций:
1. Образование кислорода из Н2О по реакции:
2Н2О → О2 + 4е- + 4Н+ (А.1)
2. Реакция растворения материала анода:
Ме → Меn+ + nе- (А.2)
Для сплавов на основе железа (ферросилид, магнетит) реакция А.2 принимает вид:
Fe → Fe2+ + 2е-